Osmose ist nichts anders als die Diffusion des Wassers. Um den osmotischen Effekt (also die Diffusion des Wassers) sichtbar zu machen, müssen wir zwischen dem Wasser und den in ihm gelösten Teilchen unterscheiden. Das können wir am besten mit einer semipermeablen Membran bewerkstelligen.
Was ist eine semipermeable Membran?
Eine semipermeable (halb-durchlässige) Membran ist in der Lage nur die Wassermoleküle passieren zu lassen. Die gelösten Teilchen können eine semipermeablen Membran nicht passieren.
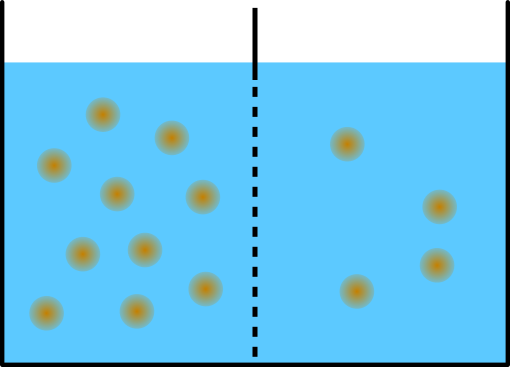
Die Abbildung zeigt die Ausgangssituation eines Osmose-Experiments. Wir haben einen mit Wasser (blau) gefüllten Behälter durch eine semipermeable Membran in zwei Kammern geteilt. Nun wurde auf der linken Seite mehr Zucker (braun) aufgelöst als in der rechten Seite. Schaue dir die Abbildung an. Auf welcher Seite ist die Konzentration vom Zucker höher?
Die Anzahl der gelösten Zuckerteilchen sinkt von links (10 Teilchen) nach rechts (4 Teilchen). Das Konzentrationsgefälle der Zuckerteilchen zeigt also von links nach rechts.
Wenn die Membran entfernt wird, setzt eine Diffusion von Zuckerteilchen von links nach rechts ein, da das Konzentrationsgefälle von links nach rechts zeigt, d. h. die Konzentration von Zucker nimmt von links nach rechts ab.(s. Abbildung)
Die Osmose, ist die Diffusion des Wassers. Bisher haben wir uns die Diffusion von Zucker angeschaut. Jetzt müssen wir an das Wasser denken. Beginnen wir mit der Konzentration von Wasser auf beiden Seiten. Auf welcher Seite herrscht eine höhere RELATIVE Konzentration des Wassers?
Es geht darum zu bestimmen, auf welcher Seite mehr Wassermoleküle pro Zuckerteilchen vorhanden sind. Die höchste relative Konzentration hat das reine Wasser ohne gelöste Stoffe. Je mehr Fremdteilchen, wie z. B. Zucker sich im Wasser auflösen, desto geringer wird die relative Konzentration von Wasser.
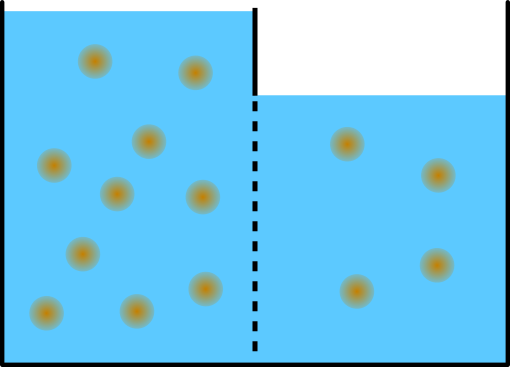
Auf der rechten Seite gibt es mehr Wassermoleküle pro Zuckerteilchen. Und das Konzentrationsgefälle des Wassers (von rechts nach links) ist genau dem Konzentrationsgefälle von Zucker entgegen gerichtet. Das Wasser möchte, genauso wie Zucker seinem Konzentrationsgefälle folgen. Das Wasser fließt also von rechts nach links und somit entgegen des Konzentrationsgefälle vom Zucker.
Die Osmose wird solange laufen bis ihr eine Gegenkraft entgegen wirkt. In unserem Beispiel kann man sagen, dass je mehr Wasser von rechts nach links fließt, desto höher steigt der Flüssigkeitsspiegel auf der linken Seite und desto tiefer sinkt sie auf der rechten Seite. Dieser Höhenunterschied produziert eine Gewichtskraft. Wenn das Gewicht des zusätzlichen Wassers auf der linken Seite groß genug ist, kann es das Wasser wieder zurück in die rechte Seite drücken. In unserem Beispiel also stoppt die Osmose, wenn das Gewicht des zusätzlichen Wassers, d.h. der Höhenunterschied auf beiden Seiten genau so groß ist, wie der osmotischen Druck von rechts nach links.
Die Osmose ist für den Wasserhaushalt einer Zelle besonders relevant. Abhängig davon in welche Lösung eine Zelle eingebracht wird, kann die Osmose eine Zelle (ohne Zellwand) schrumpfen oder platzen lassen.
Isotone Lösungen
Eine Lösung ist isoton, wenn die Konzentration der in ihr gelösten Stoffe, der Konzentration im Zellinnern gleicht. In diesem Fall ist die Menge an Wasser, das aufgrund der Osmose in die hinein Zelle fließt gleich der Wassermenge, die aus der Zelle heraus fließt. Somit fließt in der Summe kein Wasser in bzw. aus der Zelle.
Während dieser Fall den Normalfall bei tierischen Zellen darstellt, erschlaffen die meisten Pflanzen unter isotonen Bedingungen.
Hypotone Lösungen
Eine Lösung ist hypoton, wenn die Konzentration der in ihr gelösten Stoffe geringer ist als die Konzentration im Zellinnern. In diesem Fall ist die Menge an Wasser, das aufgrund der Osmose in die Zelle hinein fließt größer als die Wassermenge, die aus der Zelle heraus fließt. Somit fließt in der Summe Wasser in die Zelle. Dadurch bläht sich die Zelle auf.
Bei Zellen ohne eine Zellwand (z. B. bei tierischen Zellen) führt dies zum Aufblähen und anschließendem Platzen der Zelle. Man spricht davon, dass die Zelle lysiert. Einige Protisten, wie das Pantoffeltierchen können mit Hilfe ihrer kontraktilen Vakuolen das eingeströmte Wasser wieder herauspressen und somit ein Platzen verhindern. Bei Zellen mit einer Zellwand (z. B. bei Pflanzenzellen, Pilzen und Prokaryoten) verhindert eben diese Zellwand ein zu starkes Aufblähen. Dies ist für die Pflanzenzellen der Normalzustand, da sie durch diesen Effekt ihre Gestalt bewahren.
Hypertone Lösungen
Eine Lösung ist hyperton, wenn die Konzentration der in ihr gelösten Stoffe höher ist als die Konzentration im Zellinnern. In diesem Fall ist die Menge an Wasser, das aufgrund der Osmose in die Zelle hinein fließt geringer als die Wassermenge, die aus der Zelle heraus fließt. Somit fließt in der Summe Wasser aus der Zelle heraus. Dadurch schrumpft die Zelle.
Bei Zellen ohne eine Zellwand (z. B. tierische Zellen) führt dies in Extremfall zum Tod der Zelle. Bei Zellen mit einer Zellwand (z. B. Pflanzenzellen, Pilze, Prokaryoten und etc.) löst sich das Zellplasma von der Zellwand (Plasmolyse) was in Extremfall zum Tod der Zelle führen kann. Dieser Effekt führt auch in den Anfangsstadien zum Welken von Pflanzen.